精準治療的力量:負向超選在轉移性大腸直腸癌(mCRC)中的應用
醫療新聞
•
2025-08-25
近年來,轉移性大腸直腸癌(mCRC)治療的突破凸顯了個人化醫療的重要性。臨床醫師愈來愈依賴分子檢測來量身訂製治療取代「一體適用」的方法,藉此放大臨床效益並減少不必要的毒性。
.jpg)
什麼是「負向超選」?
負向超選(Negative Hyperselection)是一項新興的精準策略,透過排除帶有抗藥性基因變異的患者,來篩選適合使用抗EGFR 藥物(如 panitumumab、cetuximab)的族群。
此方法不僅考量傳統的 RAS 突變或tumorsidedness,加入更廣泛的生物標記來辨識最有可能受益的病患。
臨床證據
PARADIGM 試驗
- 第三期 PARADIGM:在 RAS wild-type、左側原發腫瘤的患者中,panitumumab + mFOLFOX6 與 bevacizumab + mFOLFOX6 相比,整體存活期(OS)更長。進一步於Nature Medicine發表的研究, 納入 PARADIGM試驗中的733 位病人, 檢測是否存在以下抗-EGFR耐藥性相關基因變異,包括:
- KRAS、NRAS、PTEN、EGFR 胺基端突變
- HER2、MET 擴增
- ALK、RET、NTRK1
- 符合負向超選(不帶上述變異)的患者,使用 panitumumab 的中位 OS 為 40.7 個月,顯著優於 bevacizumab 的 34.4 個月(HR 0.76, 95% CI: 0.62–0.92)。
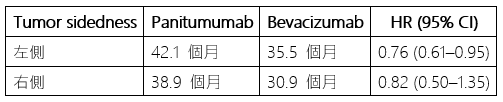
這些結果顯示,傳統標記如 RAS 狀態與腫瘤原發部位,可能不足以作為一線治療決策的依據。更廣泛的分子檢測能夠提供更精細的病人篩選,並更準確地預測治療反應。近期支持此觀點的另外一篇FIRE-3 試驗的回顧性分析(該試驗比較了 RAS 野生型患者中一線 FOLFIRI 聯合 cetuximab 與 FOLFIRI 聯合 bevacizumab 的效果)顯示,透過 次世代定序(NGS)進行的分子超精選(molecular hyperselection),可取代腫瘤原發部位,成為判斷最合適標靶治療的更準確工具。
臨床實踐:如何落實負向超選
- 透過廣泛型 NGS 檢測(腫瘤組織或液態活檢 ctDNA),不僅檢測 RAS,亦涵蓋其他與 anti-EGFR 抗藥性相關的基因變異,如 PTEN、HER2、MET 等。藉此可達成以下臨床優勢:
- 更精準的病患分層
- 提高抗 EGFR 反應率
- 避免無效治療及副作用
- 決策不再侷限於 RAS/BRAF 與腫瘤側別
結論:邁向新照護標準
負向超選開啟了 mCRC 精準治療的新篇章。透過擴大分子排除標準,醫師能更有信心鎖定真正受益的患者。隨著證據累積,負向超選有望成為臨床新常規,為轉移性大腸直腸癌患者帶來更個人化且有效的治療。
參考文獻
- Stahler A, Kind AJ, Sers C, 等. Clin Cancer Res. 2024;30(7):1256-63.
- Shitara K, Muro K, Watanabe J, 等. Nat Med. 2024;30(3):730-39.
- Watanabe J, Muro K, Shitara K, 等. JAMA. 2023;329(15):1271-82.
- Weiss L, Stintzing S, Stahler A, 等. Eur J Cancer. 2025;221:115399.









.jpg)
.jpg)

