點亮HER2超低表達乳癌的希望之光─超低表達精準檢測利器
精準醫療
•
2025-11-07
HER2標靶治療的邊界正持續被改寫,從陽性到低表達再到超低表達,對HER2檢測精度與判讀一致性提出更高要求。Trastuzumab deruxtecan在HER2低與超低表達乳癌治療中取得重大突破,重塑HER2標靶治療格局,同时也對乳癌HER2檢測提出了新的要求。考慮當前病理科醫師面臨的判讀挑戰,所以我們需要探索新的、更科學的檢測判讀方法。質譜臨床蛋白質體學技術通過內標肽絕對定量,實現高靈敏度、高特異性的多個靶點同步定量,為精準檢測提供新方案,助力乳癌個體化治療。
原文出自:mProbe 雲檢

1、DESTINY-Breast06 推動 HR 陽性晚期乳癌診療再革新
乳癌HER2標靶治療的邊界,從陽性、低表達到超低表達,不斷被打破。2025年1月27日,美國食品藥品監督管理局(FDA)擴大了trastuzumab deruxtecan(Enhertu,fam-trastuzumab deruxtecan)的適應症範圍,用於內分泌治療後激素受體陽性(HR+)、HER2超低表達晚期乳癌患者的治療。FDA最初於2019年12月批准trastuzumab deruxtecan用於HER2高表達的不可手術或轉移性乳癌,2022年8月擴大至HER2低表達乳癌,如今進一步延伸至HER2超低表達患者。
此項批准擴大基於2024年ASCO年會發表並刊登於《新英格蘭醫學雜誌》的Ⅲ期DESTINY-Breast06臨床試驗數據。1,2 繼2022年DESTINY-Breast04為HER2低表達患者開創治療新紀元後³,DESTINY-Breast06再度突破HER2治療邊界,拓展至HER2超低表達,令HER2超低表達成為乳癌診療新焦點,如何精準鑑別HER2超低表達也成為病理學家面臨的新挑戰。
本文將帶您了解trastuzumab deruxtecan革新乳癌診療標準的關鍵數據、HER2標靶治療的演進、HER2低/超低表達的挑戰,以及質譜絕對定量蛋白質體學在超低表達精準檢測中的關鍵價值。
2、HER2標靶治療的前世今生
過去根據人類表皮生長因子受體2(HER2)蛋白的表達情況,乳癌僅被分為HER2陽性與HER2陰性兩類。約15–20%的乳癌屬於HER2高表達(HER2陽性)。未歸入HER2陽性的腫瘤則被視為HER2陰性。其中HR陽性、HER2陰性型佔所有乳癌約70%。內分泌治療是HR陽性轉移性乳癌的主要一線治療方式,但在初始療效後往往效果有限,後續標準治療為化療。4,5,6
基於trastuzumab deruxtecan的臨床試驗數據,專家確定了另外兩種HER2乳癌分類:HER2低表達與HER2超低表達。HER2低表達指免疫組織化學(IHC)為1+或2+且原位雜交(ISH)陰性,而HER2超低表達則指IHC介於0至1+之間,即不完整、微弱细胞膜染色细胞>0和≤10%的情况。
HER2陽性乳癌由於HER2基因拷貝數增加,導致腫瘤細胞表面HER2蛋白過度表達,使癌細胞增殖迅速。相反,HER2陰性者HER2表達正常,惡性程度較低。HER2蛋白猶如細胞表面的天線,在HER2低或超低表達的乳癌中,HER2蛋白稀少且分布疏遠,當細胞分裂時,其中兩種HER2蛋白必須以受控的方式结合在一起,發出细胞複製信號。然而在HER2陽性乳癌中,過量的HER2蛋白會無序碰撞,導致不受控制的細胞分裂。
3、HER2分類精細化的重要性:抗HER2治療時間軸
早期HER2標靶藥物,如Trastuzumab(Herceptin)及Pertuzumab(Perjeta),能精確鎖定HER2高表達腫瘤細胞;隨後的Lapatinib(Tykerb)、Neratinib(Nerlynx)、Tucatinib(Tukysa)則透過通过与胞内酪氨酸激酶結構區域相結合,抑制其自身磷酸化,從而阻斷它們的激酶活性,即通過阻斷由表達HER2蛋白相互碰撞引發的信號来發揮作用。然而這些藥物僅對HER2陽性腫瘤有效,對HER2表達極低的患者無助益,因此HER2低或超低表達過去皆被歸為HER2陰性。
新一代HER2靶向治療藥物,如trastuzumab deruxtecan,兼具抗HER2抗體與化療藥物的雙重作用。藥物與腫瘤細胞表面HER2蛋白結合後被細胞攝入,釋放細胞毒性藥物以殺死癌細胞。這一突破促使專家重新評估過去被歸類為HER2陰性的腫瘤,確認其是否可能屬於HER2低或超低表達,並可從新型抗體偶聯藥物中受益。
4、HER2狀態如何確定
判定HER2狀態需利用乳癌手術或活檢組織樣本。病理醫師以IHC染色結果區分0至3分:0代表未檢出HER2蛋白,3代表HER2過度表達。IHC評分為2者需再進行螢光原位雜交(FISH)檢測。HER2低表達包括IHC 1分或2分且FISH陰性;IHC 0則可再區分為HER2超低表達與HER2陰性。
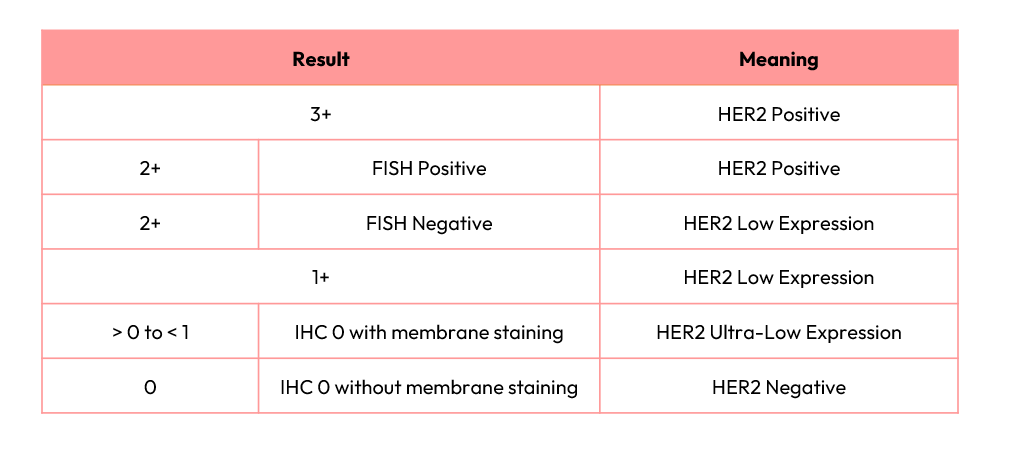
5、HER2低/超低表達對病理判讀的挑戰
在DESTINY-Breast06研究中,HER2 IHC結果須經中心實驗室確認方可入組。HER2超低表達入組條件為:地方實驗室判為IHC 0者,中心實驗室判讀為0至1+之間。此區分要求病理醫師辨別是否存在任何細胞膜染色,對臨床判讀提出更高要求。
探索性分析顯示,多數(64%)地方實驗室評為IHC 0的患者,在中心評估後被改判為HER2低表達(24%)或HER2超低表達(40%)。因此,對於HR+轉移性乳癌且IHC 0的患者,建議重新評估是否符合trastuzumab deruxtecan治療條件。7
6、HER2低/超低表達精準檢測利器──質譜絕對定量蛋白質體學
HER2表達是乳癌預後與抗HER2藥物療效的重要指標。隨著檢測精度從高表達到低表達再到超低表達,對檢測結果的準確性要求日益提高。傳統IHC受限於半定量與觀察者差異。質譜絕對定量蛋白質體學透過內標肽實現多靶點同步定量,具高靈敏度與高特異性,突破傳統瓶頸。
基於質譜絕對定量蛋白檢測方法分析173例不同IHC等級的乳癌樣本,HER2濃度隨IHC分數增加而上升(HER2 0最低,HER2 3+最高)。然而,通過質譜檢測,發現其中73%的IHC 0樣本可檢測出HER2蛋白(168–623 amol/μg)。HER2在2+與0間差異顯著(p<0.05),而2+與1+、1+與0間則無顯著差異。8
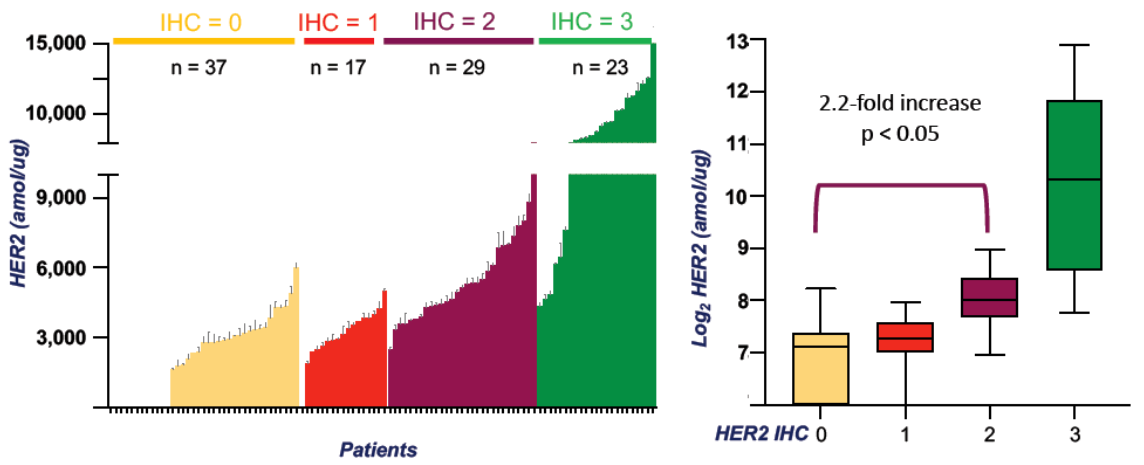
結語
HER2標靶治療的邊界正持續被改寫,從陽性到低表達再到超低表達,對HER2檢測精度與判讀一致性提出更高要求。Trastuzumab deruxtecan在HER2低與超低表達乳癌治療中取得重大突破,重塑HER2標靶治療格局,同时也對乳癌HER2檢測提出了新的要求。考慮當前病理科醫師面臨的判讀挑戰,所以我們需要探索新的、更科學的檢測判讀方法。質譜臨床蛋白質體學技術通過內標肽絕對定量,實現高靈敏度、高特異性的多個靶點同步定量,為精準檢測提供新方案,助力乳癌個體化治療。
參考資料
- Giuseppe Curigliano et al., Trastuzumab deruxtecan (T-DXd) vs physician’s choice of chemotherapy (TPC) in patients (pts) with hormone receptor-positive (HR+), human epidermal growth factor receptor 2 (HER2)-low or HER2-ultralow metastatic breast cancer (mBC) with prior endocrine therapy (ET): Primary results from DESTINY-Breast06 (DB-06). JCO 42, LBA1000-LBA1000(2024)
- Bardia A, Hu X, Dent R, et al. Trastuzumab Deruxtecan after Endocrine Therapy in Metastatic Breast Cancer. N Engl J Med. 2024;391(22):2110-2122.
- Modi S, Jacot W, Yamashita T, et al. Trastuzumab Deruxtecan in Previously Treated HER2-Low Advanced Breast Cancer. N Engl J Med. 2022;387(1):9-20.
- Ahn S, et al. HER2 status in breast cancer: changes in guidelines and complicating factors for interpretation. J Pathol Transl Med. 2020;54(1):34-44.
- Sajjadi E, et al. Improving HER2 testing reproducibility in HER2-low breast cancer. Cancer Drug Resist. 2022;5(4):882-888.
- Manohar P, et al. Updates in endocrine therapy for metastatic breast cancer. Cancer Biol Med. 2022 Feb 15; 19(2):202–212.
- Salgado RF, et al. LBA21 - Human epidermal growth factor receptor 2 (HER2)-low and HER2-ultralow status determination in tumors of patients (pts) with hormone receptor–positive (HR+) metastatic breast cancer (mBC) in DESTINY-Breast06 (DB-06). Annals of Oncology. (2024) 35 (suppl_2): 1-72. 10.1016/annonc/annonc1623.
- Fabiola C, et al. Quantitative mass spectrometry of HER2 protein levels reveals high variability within HER2 IHC grades [abstract]. In: Proceedings of the Annual Meeting of the American Association for Cancer Research 2020; 2020 Apr 27-28 and Jun 22-24. Philadelphia (PA): AACR; Cancer Res 2020;80(16 Suppl):Abstract nr 5128.









.jpg)
.jpg)

